
Autor: MUDr. Vlasta Raušová
Mnohočetný myelom (MM) je záludná nemoc. Navzdory obrovskému pokroku v jeho léčbě je vyléčení vzácné. Ještě nedávno se zdálo, že někteří z nejvýznamnějších vědců v oboru by byli rádi, kdyby se z něj podařilo udělat chronické onemocnění. Jiní si šli za vyléčením. První pokusy o vyléčení této nemoci zahrnovaly autologní a alogenní transplantace po vysokodávkované myeloablativní léčbě.
Někteří pacienti přežívali dvacet a více let, především po alogenní transplantaci. Myšlenka, že nejdůležitější součástí alogenního přístupu není vysokodávkovaná léčba, ale spíše účinek štěpu proti myelomu, který uplatňují transplantované alogenní lymfocyty, vyvolala modifikaci postupu s použitím kondicionování se sníženou intenzitou a předcházející autotransplantace. Výsledky byly povzbudivé, ale nadále se objevovaly relapsy a vyléčení bylo vzácné.
Transfuze dárcovských lymfocytů k léčbě relapsů byly krátkodobě úspěšné a byly důkazem principu, že buněčná terapie alogenními lymfocyty může vyvolat odpovědi trvající několik měsíců nebo dokonce let. Relativně krátkodobý účinek dárcovských lymfocytů byl však nespecifický a často způsoboval onemocnění štěpu a hostitele. Skutečným průlomem tedy bylo vytvoření T-lymfocytu, který by se mohl zaměřit na specifické antigeny na nádorových buňkách. Účinný T-lymfocyt s chimérickým antigenním receptorem (CAR) byl vyroben již na počátku 90. let minulého století a po určitém zpoždění byly vyvinuty CAR T-lymfocyty pro klinické použití. Od počátku 21. století až do současnosti počet klinických studií rakoviny s těmito buňkami prudce vzrostl.
U MM je nejčastějším cílem CAR T-buněčné terapie antigen maturace B lymfocytů (BCMA), ale v současné době se zkoumá mnoho dalších antigenů na myelomových buňkách. CAR T-buňky jsou modifikované ex vivo tak, aby exprimovaly chimérický receptor. Tento receptor obsahuje antigenní receptor, tj. jednořetězcový variabilní fragment (scFv), a intracelulární signální doménu T-buněčného receptoru (TCR). ScFv rozpoznává cílové nádorové buňky, zatímco intracelulární doména obsahuje různé složky pro zvýšení účinnosti a bezpečnosti. Ve většině probíhajících studií se k produkci CAR T-buněk používají autologní buňky.
Přípravky idekabtagen vikleucel (ide-cel) a ciltacabtagene autoleucel(cilta-cel) byly pro léčbu MM schváleny jak americkým Úřadem pro kontrolu potravin a léčiv, tak Evropskou lékovou agenturou, na základě dvou studií fáze II (studie KarMMa a studie CARTITUDE).
Ve studii KarMMa byl podáván idekabtagen vikleucel (ide-cel) pacientům, kteří již dříve dostávali inhibitor proteazomu, imunomodulační léky a protilátky anti-CD38 a byli refrakterní na poslední linii léčby. Po lymfodepleci (cyklofosfamid 300 mg/m2 + fludarabin 30 mg/m2 × 3) dostali nemocní CAR T-lymfocyty zacílené na BCMA. Ze 140 zařazených pacientů bylo takto léčeno 128 osob, medián věku činil 61 let, medián předchozích linií terapie 6 (84 % bylo triple- a 26 % pentarefrakterních). Při mediánu doby sledování 11,3 měsíce dosáhla celková míra odpovědi 73 % a medián času do progrese onemocnění 8,6 měsíce.
Aktuálně jsou k dispozici i dlouhodobější výsledky ze studie fáze Ib/II CARTITUDE-1, která zkoumá přípravek označovaný JNJ-68284528 (JNJ-4528) – rovněž CAR T-buněčnou terapii zaměřenou proti BCMA. Spektrum nežádoucích příhod bylo obdobné jako v předchozích studiích, pouze ve 2 případech se rozvinul syndrom uvolnění cytokinů 3., resp. 5. stupně (po 99 dnech trvání 4. stupně). Celková odpověď činila 100 %, z toho 22 nemocných (76 %) dosáhlo sCR (stringentní kompletní remise), 6 (21 %) VGPR (velmi dobrá částečná odpověď) a 1 PR (částečná odpověď). Nejdůležitější v této studii je fakt, že 26 z 29 pacientů je stále bez známek progrese – po 6měsíčním sledování se jedná o 93 %, po 9 měsících o 90 % a zatím nejdelší odpověď trvá 15 měsíců. Všech 16 pacientů se sCR a VGPR (14 případů sCR, 2 případy VGPR) hodnocených po 6 měsících vykazovalo negativitu minimálního reziduálního onemocnění.
Nedávné aktualizované retrospektivní srovnání ukázalo lepší odpověď (míra objektivní odpovědi 97,9 %; stringentní kompletní odpověď 82,5 %), přežití bez progrese (62% snížení rizika) a celkové přežití (57% snížení rizika) u cilta-celu ve srovnání s ide-celem.
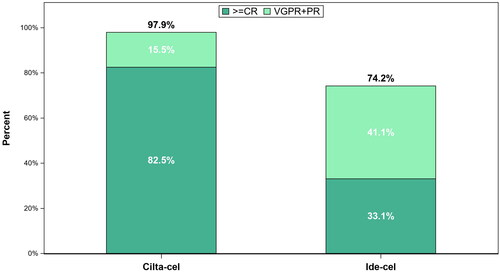 Overall response rates prior to adjustment for cilta-cel and ide-cel.
Overall response rates prior to adjustment for cilta-cel and ide-cel.
CR=complete response; PR=partial response; VGPR=very good partial response
Převzato z: Martin T., Curr Med Res Opin. 2023; 39(1)
Jiné studie zahrnující menší počet pacientů rovněž prokázaly působivé krátkodobé výsledky. Ačkoli jsou tyto výsledky povzbudivé, počet pacientů vyšetřených v jednotlivých studiích není dostatečně vysoký, aby poskytl spolehlivé informace o vlivu prognostických faktorů, jako je přítomnost extramedulárního onemocnění (EMD) nebo vysoce rizikové cytogenetiky.
V tomto čísle časopisu Haematotogica se Gagelmann a kol. pokoušejí o retrospektivní analýzu těchto důležitých prognostických faktorů shromážděním výsledků z dostupných klinických studií s CAR T-buňkami. Ze 769 prověřených článků nalezli 17, které zahrnovaly 723 silně předléčených pacientů s relabovaným nebo refrakterním MM s údaji obsahujícími dostatek informací o těchto prognostických faktorech. Z komplexní statistické analýzy vyplynulo, že EMD nebránilo odpovědi, ale přežití bez progrese bylo o 44 % kratší a celkové přežití kratší kvůli EMD. Pacienti s vysokým cytogenetickým rizikem si vedli ještě hůře ve srovnání s pacienty bez vysokého rizika. Riziko žádné odpovědi se zvýšilo o 14 %, riziko pozitivity minimálního reziduálního onemocnění o 23 % a riziko progrese/relapsu se zvýšilo o 70 %, což ovlivnilo celkové přežití, které se významně zkrátilo.
Zdá se tedy, že v současné době používaná CAR T buněčná terapie nepřekonává špatný prognostický dopad EMD nebo vysoce rizikové cytogenetiky; nové přístupy jsou proto opodstatněné. U většiny zařazených pacientů byl cílem CAR T buněčné terapie BCMA a byly použity autologní buňky. Probíhající studie využívající CAR T buňky namířené proti jiným antigenům, jako je orphan G protein-coupled receptor GPRC5, dvousměrné CAR T buňky, alogenní CAR T buňky, NK buňky (natural killers) nebo CAR NK buňky, mohou ukázat lepší odpověď a výsledky u vysoce rizikových pacientů s relabovaným a refrakterním myelomem.
Budoucí studie by měly CAR T buněčnou terapii přesunout do časnějších stadií onemocnění. Myelom s EMD a vysoce rizikovou cytogenetikou může být dobře léčen již v počáteční fázi pomocí CAR T-buněk a odpovědi mohou být konsolidovány dalšími léčebnými postupy, jako jsou bispecifické protilátky nebo alogenní transplantace. Cílem musí být vyléčení.
Reference:
1/ Gahrton G. Et al., CAR T-cell treatment of high-risk multiple myeloma: will there be a cure?, Haematologica, Vol. 108 No. 10 (2023): October, 2023 https://doi.org/10.3324/haematol.2023.282896
2/ Gagelmann N. et al., Impact of high-risk disease on the efficacy of chimeric antigen receptor T-cell therapy for multiple myeloma: a metaanalysis of 723 patients. Haematologica. 2023; 108(10):2799-2802. https://doi.org/10.3324/haematol.2022.282510
3/ Munshi NC. et al., Idecabtagene vicleucel in relapsed and refractory multiple myeloma, N Engl J Med. 2021;384(8):705-716.
4/ Berdeja JG. et al., Ciltacabtagene autoleucel, a B-cell maturation antigen-directed chimeric antigen receptor T-cell therapy in patients with relapsed or refractory multiple myeloma (CARTITUDE-1): a phase 1b/2 open-label study. Lancet. 2021;398(10297):314-324.
5/ Berdeja JG., Update of CARTITUDE-1: A phase Ib/II study of JNJ-4528, a B-cell maturation antigen (BCMA)-directed CAR-T-cell therapy, in relapsed/refraktory multiple myeloma. ASCO, 2020.
6/ Martin T. et al., Updated results from a matching-adjusted indirect comparison of efficacy outcomes for ciltacabtagene autoleucel in CARTITUDE-1 versus idecabtagene vicleucel in KarMMa for the treatment of patients with relapsed or refractory multiple myeloma. Curr Med Res Opin. 2023; 39(1):81-89. https://doi.org/10.1080/03007995.2022.2139052


